T 3.5 Odpowiedzi do zadań
Układ okresowy pierwiastków
Zadanie 1
Poniżej przedstawiono schemat klatkowy określający konfigurację elektronową pierwiastka X.
Uzupełnij poniższą tabelę – wpisz symbol pierwiastka X, dane dotyczące jego położenia w układzie okresowym oraz symbol bloku konfiguracyjnego (energetycznego), do którego należy pierwiastek X.
| Symbol pierwiastka | Numer okresu | Numer grupy | Symbol bloku |
| Na | 3 | 1 | s |

Zadanie 2
Poniżej przedstawiono schemat klatkowy określający konfigurację elektronową trójdodatniego kationu X3+.
Uzupełnij poniższą tabelę – wpisz symbol pierwiastka X, dane dotyczące jego położenia w układzie okresowym oraz symbol bloku konfiguracyjnego (energetycznego), do którego należy pierwiastek X.
| Symbol pierwiastka | Numer okresu | Numer grupy | Symbol bloku |
| Al | 3 | 13 | p |

Zadanie 3
Poniżej przedstawiono konfigurację elektronową atomów w stanie podstawowym czterech pierwiastków.
- 1s2 2s2 2p6 3s23p64s2 3d104p2
- 1s2 2s2 2p6 3s2 3p6 4s2
- 1s2 2s2 2p6 3s2 3p6 3d10 4s1
- 1s2 2s2 2p6 3s2 3p6 3d6 4s2
Wpisz do tabeli symbole bloków konfiguracyjnych (energetycznych), do których należą te pierwiastki.
| Pierwiastek | 1 | 2 | 3 | 4 |
| Symbol bloku konfiguracyjnego | p | s | d | d |

Zadanie 4
Z konfiguracji elektronowej atomu (w stanie podstawowym) pierwiastka X wynika, że w tym atomie:
- elektrony rozmieszczone są na trzech powłokach elektronowych
- na podpowłoce 3p są dwa elektrony sparowane.
Uzupełnij poniższą tabelę. Wpisz symbol chemiczny pierwiastka X, dane dotyczące jego położenia w układzie okresowym oraz symbol bloku konfiguracyjnego (energetycznego), do którego należy ten pierwiastek.
| Symbol pierwiastka | Numer okresu | Numer grupy | Symbol bloku |
| S | 3 | 16 | p |

Zadanie 5
Z konfiguracji elektronowej atomu (w stanie podstawowym) pierwiastka X wynika, że w tym atomie:
- elektrony rozmieszczone są na czterech powłokach elektronowych
- na podpowłoce 3d oraz 4s jest łącznie jeden niesparowany elektron
- liczba elektronów na podpowłoce 3d jet większa od liczby elektronów na podpowłoce 4s
Uzupełnij poniższą tabelę. Wpisz symbol chemiczny pierwiastka X, dane dotyczące jego położenia w układzie okresowym oraz symbol bloku konfiguracyjnego (energetycznego), do którego należy ten pierwiastek.
| Symbol pierwiastka | Numer okresu | Numer grupy | Symbol bloku |
| Cu | 4 | 11 | d |

Zadanie 6
Uzupełnij poniższe zdania ー wybierz i podkreśl jedno właściwe określenie spośród podanych w każdym nawiasie.
Pierwiastki w układzie okresowym są uporządkowane zgodnie z rosnącą liczbą atomową (porządkową), co oznacza, że liczba (protonów /neutronów) wzrasta zawsze o jeden. Inaczej jest w przypadku liczby (protonów / nukleonów), która wzrasta nieregularnie. Większość pierwiastków występuje w przyrodzie z kilkoma rodzajami jąder ー nazywamy je izotopami. Nuklidy to rodzaje atomów z jądrem o określonej liczbie protonów i (elektronów / neutronów). Nuklidy tego samego pierwiastka nazywamy (izotopami / izomerami).

Zadanie 7
Poniżej przedstawiono fragment uproszczonego układu okresowego pierwiastków.
Oceń prawdziwość poniższych informacji w odniesieniu do pierwiastków znajdujących się w tym fragmencie układu okresowego. Zaznacz P, jeśli informacja jest prawdziwa, albo F – jeśli jest fałszywa.
| 1 | Strzałka I wskazuje kierunek wzrostu promieni atomów pierwiastków znajdujących się w tym samym okresie. | P | F |
| 2 | Strzałka II wskazuje kierunek wzrostu wartości pierwszej energii jonizacji pierwiastków w tej samej grupie. | P | F |
| 3 | Wzrost aktywności metali znajdujących się w tej samej grupie oznacza kierunek strzałki II | P | F |
| 4 | Wzrost ładunku jądra atomowego pierwiastków jest zgodny zarówno z kierunkiem strzałki I jak i II | P | F |

Zadanie 8
Poniżej przedstawiono fragment uproszczonego układu okresowego pierwiastków.
Oceń prawdziwość poniższych informacji w odniesieniu do pierwiastków znajdujących się w tym fragmencie układu okresowego. Zaznacz P, jeśli informacja jest prawdziwa, albo F – jeśli jest fałszywa.
| 1 | Strzałka I wskazuje kierunek wzrostu maksymalnej wartościowości pierwiastków względem tlenu. | P | F |
| 2 | Strzałka I wskazuje kierunek wzrostu maksymalnej wartościowości pierwiastków względem wodoru. | P | F |
| 3 | Wodorki grupy 14 można opisać wzorem ogólnym XH4 gdzie X jest pierwiastkiem grupy 14 | P | F |
| 4 | Charakter zasadowy pierwiastków grupy 1 rośnie zgodnie kierunkiem strzałki I | P | F |

Zadanie 9
Spośród wymienionych określeń zaznacz wszystkie, które są poprawnym dokończeniem zdania.
W drugim okresie układu okresowego w grupach 1.–2. i 13.–17. ze wzrostem liczby atomowej pierwiastków następuje wzrost (liczby elektronów walencyjnych / liczby powłok elektronowych w atomach / elektroujemności pierwiastków / promieni atomów).

Zadanie 10
W układzie okresowym pierwiastków wyróżnia się 4 bloki konfiguracyjne:
Zaznacz znakiem x na poniższym schemacie fragmentu układu okresowego wszystkie pierwiastki, które należą do bloku p, a ich atomy w powłoce walencyjnej (w stanie podstawowym) mają dokładnie trzy elektrony niesparowane.
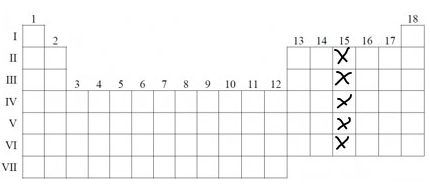

Zadanie 11
Określ tendencję zmiany (wzrasta, maleje) promienia atomowego i elektroujemności pierwiastków bloków konfiguracyjnych s i p w grupach układu okresowego pierwiastków.
W grupie w miarę wzrostu liczby atomowej promień atomowy rośnie,
a elektroujemność maleje.

Zadanie 12
Na rysunku przedstawiono schemat układu okresowego pierwiastków (bez lantanowców i aktynowców), na którym umieszczono strzałki A i B odpowiadające kierunkom zmian wybranych wielkości charakteryzujących pierwiastki chemiczne.
Podkreśl wszystkie wymienione poniżej wielkości, których wzrost wskazują strzałki oznaczone literami A i B.
1. Dla pierwiastków grupy 1. grupy strzałka A wskazuje kierunek wzrostu
najwyższej wartościowości; promienia atomowego; ładunku jądra
2. Dla pierwiastków grup 1.–2. i 13.–17. okresu III strzałka B wskazuje kierunek wzrostu
wartości pierwszej energii jonizacji, promienia atomowego, charakteru niemetalicznego

Zadanie 13
Na poniższym schemacie układu okresowego pierwiastków (bez lantanowców i aktynowców) zaznaczono położenie trzech pierwiastków oznaczonych numerami I, II oraz III.
| Informacja | P/F |
| Promień pierwiastka II jest większy od promienia pierwiastka III. | F |
| Pierwiastek I tworzy wodorek o wzorze ogólnym XH a pierwiastek III wodorek o wzorze ogólnym HX. | P |
| Tlenek pierwiastka I ma charakter zasadowy a pierwiastka II kwasowy. | P |

Zadanie 14
Na podstawie budowy atomów pierwiastków należących do 16. i 17. grupy i trzeciego okresu układu okresowego uzupełnij poniższe zdania. Wybierz i podkreśl jedno z określeń podanych w nawiasie, tak aby powstały zdania prawdziwe.
Jądro atomu fluorowca ma ładunek ( mniejszy / większy ) niż jądro atomu tlenowca.
Atom fluorowca ma ( mniejszy / większy ) promień atomowy niż atom tlenowca.
Tlenowiec jest ( bardziej / mniej ) aktywny chemicznie od fluorowca.

Zadanie 15
Przeanalizuj położenie chloru w układzie okresowym pierwiastków i oceń prawdziwość poniższych zdań. Wpisz do tabeli literę P, jeżeli zdanie jest prawdziwe, lub literę F, jeśli jest fałszywe.
| Zdanie | P/F | |
| 1 | Chlor jest pierwiastkiem bloku p i posiada w stanie podstawowym dwa elektrony niesparowane na podpowłoce p. | F |
| 2 | Chlor jest najaktywniejszym pierwiastkiem w swojej grupie. | F |
| 3 | Promień atomu chloru jest mniejszy od promienia atomu bromu, a większy od promienia atomy fluoru | P |

Zadanie 16
Pierwsza energia jonizacji (Ej) to minimalna energia potrzebna do oderwania jednego elektronu od obojętnego atomu. Na poniższym wykresie przedstawiono zmiany pierwszej energii jonizacji pierwiastków uszeregowanych według liczb atomowych.
Oceń prawdziwość poniższych zdań i uzupełnij tabelę. Wpisz literę P, jeżeli uznasz zdanie za prawdziwe, lub literę F, jeżeli uznasz je za fałszywe.
| Zdanie | P/F | |
| 1 | W szeregu pierwiastków: sód, magnez, krzem i fosfor wraz ze wzrostem liczby atomowej obserwujemy zależność polegającą na tym, że im więcej elektronów znajduje się na powłoce zewnętrznej, tym większa jest wartość pierwszej energii jonizacji. | P |
| 2 | Największe wartości pierwszej energii jonizacji mają w każdym okresie gazy szlachetne | P |
| 3 | Azot ma większy promień od węgla i dlatego jego pierwsza energia jonizacji jest większa | F |

Zadanie 17
Pierwiastek chemiczny o liczbie atomowej 31 znajduje się w 13 grupie i IV okresie układu okresowego pierwiastków chemicznych, czyli w bloku energetycznym p a rozmieszczenie elektronów walencyjnych w atomie tego pierwiastka chemicznego można przedstawić (z uwzględnieniem powłok i podpowłok elektronowych): 4s24p1 .

Zadanie 18
Podane tlenki uporządkuj według wzrastającego charakteru zasadowego:
K2O, MgO, Na2O, Rb2O, Al2O3
Al2O3, MgO, Na2O, K2O, Rb2O

Zadanie 19
Pewien pierwiastek (E) tworzy wodorek typu EH3, jego atom ma 4 powłoki elektronowe oraz spośród elektronów walencyjnych 3 są niesparowane w stanie podstawowym.
| Symbol pierwiastka | As |
| Wzór tlenku tworzonego przez ten pierwiastek | As2O5 |

Zadanie 20
Uzupełnij tabelę:
| Symbol pierwiastka | Cr |
| Blok energetyczny | d |
| Zapis skrócony konfiguracji | [Ar]4s13d5 |
| Liczba elektronów niesparowanych | 6 |
| Zapis graficzny elektronów walencyjnych | 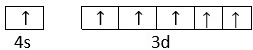 |
| Wzór tlenku na najwyższym stopniu utlenienia | CrO3 |
| Liczba powłok elektronowych jonu Cr3+ | 3 |