T 2.4 Zadania typy maturalnego
Elektrony w atomie
Zadanie 1
Pierwiastek X należy do III okresu. W stanie podstawowym może tworzyć cząsteczki XCl3 a w stanie wzbudzonym XCl5.
- Podaj symbol pierwiastka X: ………………………………………………………………………………
- Uzupełnij zdania podkreślając właściwe słowo.
Liczba elektronów walencyjnych pierwiastka X wynosi 3 / 5. Liczba elektronów niesparowanych w stanie podstawowym to 3 / 5 a w stanie wzbudzonym 3 / 5.

Zadanie 2
Pewien pierwiastek posiada cztery elektrony walencyjne opisane główną liczbą kwantową równą 5. Elektrony walencyjne tego pierwiastka zajmują orbitale s, i p. W stanie podstawowym tworzy tlenek, w którym maksymalny stopień utlenienia tego pierwiastka jest równy IV.
- Podaj symbol pierwiastka X: …………………………………………………………………….………
- Podaj zapis graficzny powłoki walencyjnej pierwiastka X: ………………………………………

Zadanie 3
Jon prosty pierwiastka X posiada konfigurację elektronową argonu. Proces tworzenia jonu prostego można opisać równaniem: X + 2eー = X2ー
Podaj symbol pierwiastka X: ……………………………………………………………..………………………….

Zadanie 4
German jest twardym, błyszczącym, srebrzystoszarym półmetalem służącym między innymi do wytwarzania półprzewodników.
Uzupełnij zdania, które opisują budowę elektronową tego pierwiastka.
Elektrony walencyjne germanu znajdują się na …………….. powłoce elektronowej. Pierwiastek ten w stanie podstawowym posiada ………………… elektrony niesparowane a w stanie wzbudzonym …………
Jego elektron o najwyższej energii w stanie podstawowym zajmuje podpowłokę ………………………………….

Zadanie 5
Zidentyfikuj pierwiastki na podstawie podanych informacji wpisując odpowiedni symbol do tabeli.
| 1 | Elektrony walencyjne tego pierwiastka posiadają następująca konfigurację elektronową: 4s23d10 | |
| 2 | Zapis graficzny konfiguracji elektronowej tego pierwiastka opisujący elektrony walencyjne jest następujący: 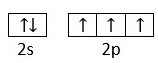 | |
| 3 | Dwudodatni kation tego pierwiastka posiada konfigurację elektronową argonu |

Zadanie 6
Podaj symbole pierwiastków o liczbach atomowych od 1 do 42 spełniających warunek:
Liczba elektronów walencyjnych danego pierwiastka jest równa głównej liczbie kwantowej opisującej elektrony walencyjne danego pierwiastka w stanie podstawowym:
………………………………………………………………………………………………………………………………

Zadanie 7
Liczba atomowa pierwiastka X jest równa liczbie masowej atomu fosforu.
Podaj symbol pierwiastka X oraz symbole podpowłok zajmowanych przez jego elektrony walencyjne.
| Podaj symbol pierwiastka X | |
| Symbole podpowłok zajmowanych przez jego elektrony walencyjne |

Zadanie 8
Podaj symbol pierwiastka, którego elektrony walencyjne opisano za pomocą następujących liczb kwantowych:
| Pierwiastek X | ||||
| n | l | m | ms | |
| Elektron 1 | 2 | 0 | 0 | ½ |
| Pierwiastek Y | ||||
| Elektron 1 | 4 | 0 | 0 | ½ |
| Elektron 2 | 4 | 0 | 0 | -½ |
| Elektron 3 | 3 | 2 | -2 | ½ |
| Pierwiastek Z | ||||
| Elektron 1 | 3 | 0 | 0 | ½ |
| Elektron 2 | 3 | 0 | 0 | -½ |
| Elektron 3 | 3 | 1 | -1 | ½ |
| Symbol pierwiastka X: | ||||
| Symbol pierwiastka Y: | ||||
| Symbol pierwiastka Z: |

Zadanie 9
Suma elektronów walencyjnych pierwiastków X i Y jest równa liczbie elektronów niesparowanych atomu chromu. Ustal symbole pierwiastków X i Y jeśli wiesz, że pierwiastek X ma taką samą liczbę elektronów sparowanych i niesparowanych a ponadto oba pierwiastki należą do okresu trzeciego.
Podaj symbol pierwiastka X: ………………………………………………………………………………….………
Podaj symbol pierwiastka Y: ………………………………………………………………………………………….

Zadanie 10
Pierwiastek X posiada w rdzeniu atomowym 28 elektronów. Jego 7 elektronów walencyjnych znajduje się na czwartej powłoce.
Podaj symbol pierwiastka X: ………………………………………………………………………………………….

Zadanie 11
Atomy pierwiastka X tworzą jony X2+ o konfiguracji elektronowej (w stanie podstawowym)
1s2 2s2 2p63s23p6
Przedstaw konfigurację elektronową atomu (w stanie podstawowym) pierwiastka X. Podkreśl ten fragment konfiguracji elektronowej, który dotyczy elektronów zewnętrznej powłoki.
………………………………………………………………………………………………………………………………

Zadanie 12
Wpisz do tabeli symbole pierwiastków chemicznych, których atomy w stanie podstawowym mają poniżej przedstawione konfiguracje elektronów walencyjnych.
| Konfiguracja elektronów walencyjnych | 3d10 4s1 | 6s2 6p2 | 3d3 4s2 |
| Symbol pierwiastka |

Zadanie 13
Konfiguracja elektronów w pewnym kationie kobaltu w stanie podstawowym jest następująca:
1s2 2s2 2p6 3s2 3p6 3d6
Napisz wzór opisanego kationu kobaltu oraz przedstaw graficznie konfigurację elektronów trzeciej powłoki w tym kationie w stanie podstawowym.
| Wzór kationu | Graficzny zapis konfiguracji elektronów trzeciej powłoki |

Zadanie 14
Elektrony walencyjne w atomach (w stanie podstawowym) pewnego pierwiastka, którego symbol oznaczono umownie literą X, mają następującą konfigurację:
4s2 4p5
Oceń, czy poniższe informacje są prawdziwe. Zaznacz P, jeśli informacja jest prawdziwa, albo F – jeśli jest fałszywa.
| 1. | Pierwiastek X jest metalem. | P | F |
| 2. | Pierwiastek X tworzy kationy proste o wzorze ogólnym X+ | P | F |
| 3. | Maksymalna wartościowość, jaką pierwiastek X przyjmuje w związkach chemicznych, jest równy VII. | P | F |

Zadanie 15
Żelazo tworzy kationy Fe2+ oraz Fe3+.
a) Określ, ile elektronów i z jakiej podpowłoki albo podpowłok oddaje atom żelaza, tworząc kation Fe2+. Dokończ poniższe zdanie, wpisując liczbę elektronów i symbol odpowiedniej podpowłoki lub podpowłok.
Tworzenie kationu Fe2+ oznacza oddanie przez atom żelaza: ………………………………………………………
b) Uzupełnij poniższą tabelę, wpisując schemat klatkowy konfiguracji elektronów walencyjnych jonu Fe3+ w stanie podstawowym oraz wartości głównej liczby kwantowej n i pobocznej liczby kwantowej l dla niesparowanych elektronów w tym jonie.
| Schemat klatkowy elektronów walencyjnych | Główna liczba kwantowa n | Poboczna liczba kwantowa l |

Zadanie 16
Podaj liczbę elektronów walencyjnych jonu Cr2+ w stanie podstawowym, zajmujących wyłącznie powłokę elektronową opisaną główną liczbą kwantową n=3.
………………………………………………………………………………………………………………………………

Zadanie 17
W stanie podstawowym atom fosforu ma trzy niesparowane elektrony.
Uzupełnij zdania. Wybierz i podkreśl symbol typu podpowłoki oraz wartość głównej i pobocznej liczby kwantowej spośród podanych w nawiasach.
Niesparowane elektrony atomu fosforu w stanie podstawowym należą do podpowłoki typu (s / p / d). Główna liczba kwantowa n opisująca stan tych elektronów wynosi (2 / 3 / 4), a poboczna liczba kwantowa l jest równa (0 / 1 / 2 / 3).

Zadanie 18
Z konfiguracji elektronowej atomu (w stanie podstawowym) pierwiastka X wynika, że w tym atomie:
- elektrony rozmieszczone są w czterech powłokach elektronowych
- elektrony walencyjne rozmieszczone są w dwóch powłokach elektronowych
- liczba elektronów walencyjnych jest równa liczbie elektronów niesparowanych atomu żelaza
a) Uzupełnij poniższą tabelę. Wpisz symbol pierwiastka X oraz dane dotyczące jego położenia w układzie okresowym.
| Symbol pierwiastka | Numer okresu | Numer grupy |
b) Napisz fragment konfiguracji elektronowej atomu pierwiastka X opisujący rozmieszczenie elektronów walencyjnych w podpowłokach.
………………………………………………………………………………………………………………………………
c) Dla jednego z niesparowanych elektronów walencyjnych podaj wartości dwóch charakteryzujących go liczb kwantowych: głównej i pobocznej. Ich wartości wpisz do tabeli.
| Liczba kwantowa | Główna liczba kwantowa (n) | Poboczna liczba kwantowa (l) |
| Wartość liczb kwantowych |

Zadanie 19
Z konfiguracji elektronowej atomu (w stanie podstawowym) pierwiastka X wynika, że w tym atomie:
• elektrony rozmieszczone są na czterech powłokach elektronowych
• na podpowłoce 3d liczba elektronów niesparowanych jest trzy razy mniejsza od liczby elektronów sparowanych.
a) Uzupełnij poniższą tabelę – wpisz symbol pierwiastka X, dane dotyczące jego położenia w układzie okresowym oraz symbol bloku konfiguracyjnego (energetycznego), do którego należy pierwiastek X.
| Symbol pierwiastka | Numer okresu | Numer grupy |
b) Zapisz konfigurację elektronową (stosując schematy klatkowe) elektronów walencyjnych, atomu pierwiastka X w stanie podstawowym. W zapisie tym uwzględnij numery powłok i symbole podpowłok. Podkreśl ten fragment konfiguracji, który nie występuje w konfiguracji elektronowej jonu X2+ (stan podstawowy).
………………………………………………………………………………………………………………………………

Zadanie 20
Skrócona konfiguracja elektronowa dla wanadu jest następująca: [Ar] 3d3 4s2. Dla jednego z niesparowanych elektronów walencyjnych podaj wartości dwóch charakteryzujących go liczb kwantowych: głównej i pobocznej. Ich wartości wpisz do tabeli.
| Liczba kwantowa | Główna liczba kwantowa [n] | Poboczna liczba kwantowa [l] |
| Wartości liczb kwantowych |