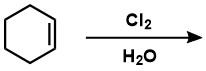Zaczynamy od przerobienia teorii, po którą zapraszam tutaj : Wzory w chemii organicznej
Kluczowe punkty, nad którymi się skupimy pod kątem Olimpiady Chemicznej :
➦ Jakich wzorów używa się w chemii organicznej i jakie są ,,wskazania” do stosowania każdego z nich?
➦ Wzory sumaryczne, strukturalne, półstrukturalne i szkieletowe – jakie są różnice?
➦ Potrafisz konwertować (zamieniać) jeden wzór na inny
Kiedy używamy dany wzór?
Wzór sumaryczny używamy do obliczeń stechiometrycznych. Używamy go też, kiedy chcemy przeanalizować co się zmieniło w danej reakcji czyli jakie atomy odeszły, a jakie się przyłączyły do naszej cząsteczki, dzięki czemu możemy ,,odgadnąć” strukturę produktu.
Wzory strukturalne stosuje się najrzadziej, ponieważ są najbardziej czasochłonne. Najlepiej stosować je wybiórczo (czyli tylko w tym rejonie cząsteczki, gdzie dzieje się akcja) w brudnopisie, kiedy chcemy dokładnie ustalić, co się wydarzyło w równaniu reakcji albo jesteśmy akurat na etapie kombinowania, co dzieje się w reakcji.
Wzory szkieletowe są najszybsze i stosujemy je w związkach cyklicznych oraz długich łańcuchach albo rozbudowanych cząsteczkach. Uwaga – ich stosowanie wiąże się z pewnym ryzykiem (np. zrobisz o jeden węgiel za dużo/za mało i masz cały wzór do wyrzucenia)!
Wzory półstrukturalne to taki idealny kompromis, najczęściej stosuje się w łańcuchu bocznym cząsteczki cyklicznej, albo gdy jest nieduża cząsteczka liniowa.
Zadanie 1 – Podaj wzór sumaryczny tej cząsteczki.
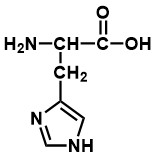
Odpowiedź : C6H9N3O2
Zadanie 2 – Ketamina, której strukturę pokazano poniżej to wielofunkcyjny organiczny związek chemiczny, substancja psychoaktywna klasyfikowana jako dysocjant psychodeliczny. Stosowana jako lek w medycynie i weterynarii do znieczulania przedoperacyjnego. Jeden z jej enancjomerów, S-ketamina, jest stosowana do leczenia depresji. Podaj wzór sumaryczny ketaminy.
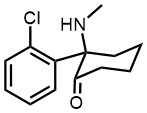
Odpowiedź : C13H16ClNO
Zadanie 3 – Napisz równanie reakcji spalania całkowitego prostaglandyny E1 , której strukturę przedstawiono poniżej. Reakcja spalania to reakcja danego związku z tlenem w warunkach zwiększonej temperatury. Mówimy o spalaniu całkowitym, jeśli produktami reakcji są tlenek węgla(IV) oraz woda.
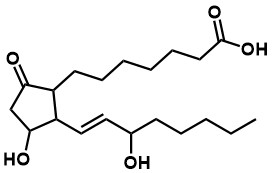
Odpowiedź :
C20H34O5 + 26O2 ⟶ 20CO2 + 17H2O
Zadanie 4 – Narysuj wzory szkieletowe dla przedstawionych poniżej cząsteczek.
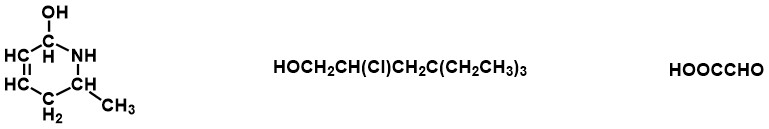
Odpowiedź :
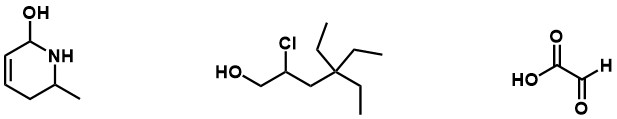
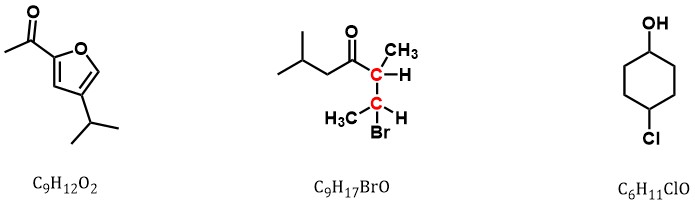
Zadanie 5 – Centrum stereogeniczne to taki atom (najczęściej) węgla, który ma cztery różne podstawniki. Czy spośród pokazanych niżej cząsteczek, któraś zawiera takie centrum? Jeśli je znajdziesz, to oznacz je gwiazdką *. Przy okazji podaj wzory sumaryczne tych związków.
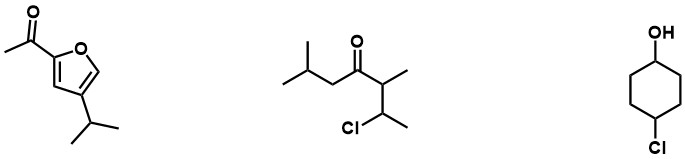
Odpowiedź : Centrum stereogeniczne, a nawet dwa, znajdziemy w drugiej cząsteczce. Zostały oznaczone na czerwono.
Zadanie 6 – Zróbmy także przykład z Olimpiady. Poniższy wycinek pochodzi z 63 edycji, II etapu : zadanie 5. Na tym wycinku widzimy wzory szkieletowe trzech cząsteczek. Idąc od góry podaj wzór : półstrukturalny, strukturalny i sumaryczny dla danej cząsteczki.
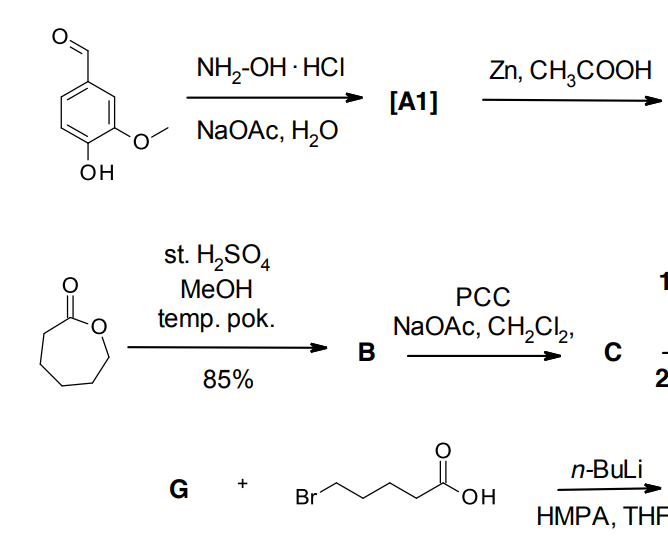
Odpowiedź :
Zadanie 7 – Napisz równanie reakcji miareczkowania podanej poniżej kwasu karboksylowego, wiedząc że typowa reakcja kwasu karboksylowego z wodorotlenkiem sodu przebiega w sposób pokazany poniżej. Kwasy karboksylowe mają wzór ogólny RCOOH, gdzie R oznacza resztę cząsteczki.
CH3COOH + NaOH ⟶ CH3COONa + H2O
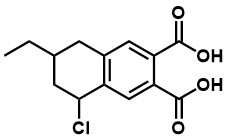
Odpowiedź :
Wzór sumaryczny kwasu to C14H15ClO4 i zawiera on dwie grupy karboksylowe (COOH), które w tym momencie tylko nas interesują, ponieważ to one (tak musimy założyć) reagują z NaOH. Można zatem ten kwas zapisać i reakcję zapisać jako :
R(COOH)2 + 2NaOH ⟶ R(COONa)2 + 2H2O
Zadanie 8 – Kluczową umiejętnością w olimpijskich zadaniach jest zidentyfikowanie ,,jakie atomy doszły albo odeszły od naszej cząsteczki”, ponieważ dzięki temu możemy podejrzewać :
- gdzie zaszła reakcja?
- w jaki sposób zaszła reakcja i co może powstać jako produkt (lub też są zadania w drugą stronę, gdzie musimy wykombinować co było substratem).
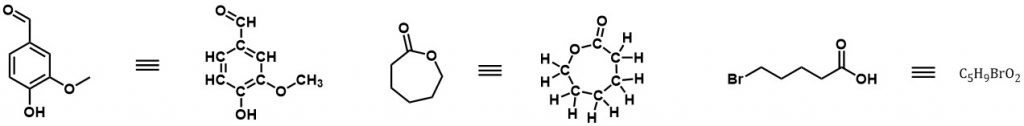
Uzupełnij wzory sumaryczne w podanych schematach syntezy.

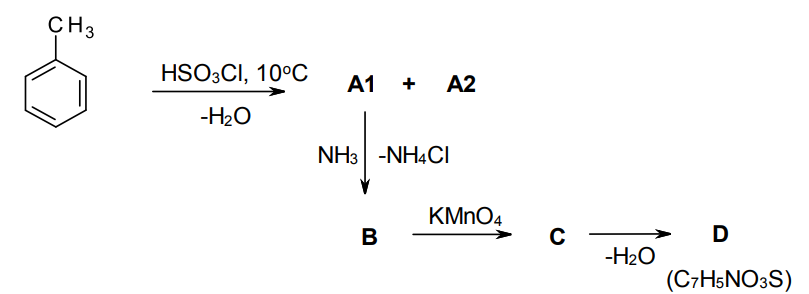
Zadanie 9 – To samo zobaczymy teraz na przykładzie zadania 4 z 58 edycji, II etapu Olimpiady Chemicznej. Komentarz : na potrzeby tego zadania zignoruj zupełnie związek A2, tak jakby w pierwszej reakcji powstał tylko związek A1. Podaj wzór sumaryczny związku A1, B oraz C. Związek B zawiera jeden atom azotu.
Zadanie 10 – Spróbuj ustalić wzór produktu (C6H11ClO)