Moduł 1,
Lekcja 1
W trakcie
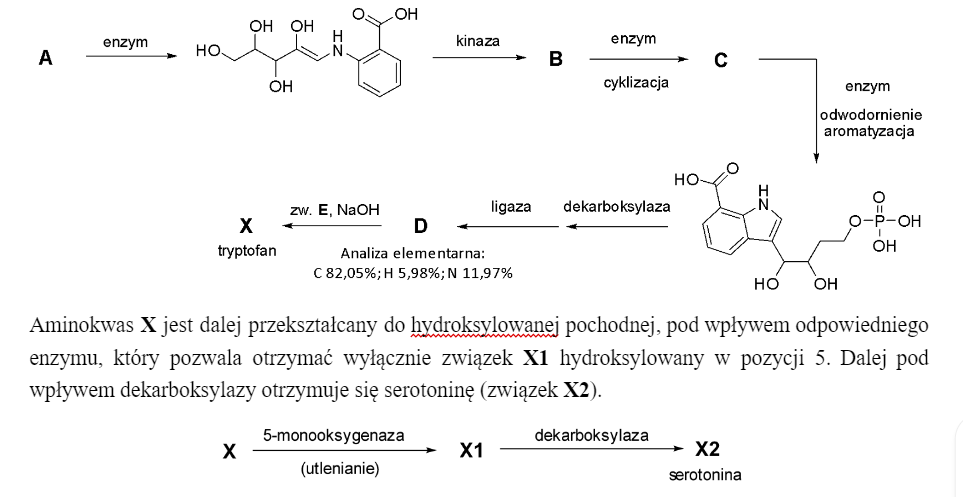
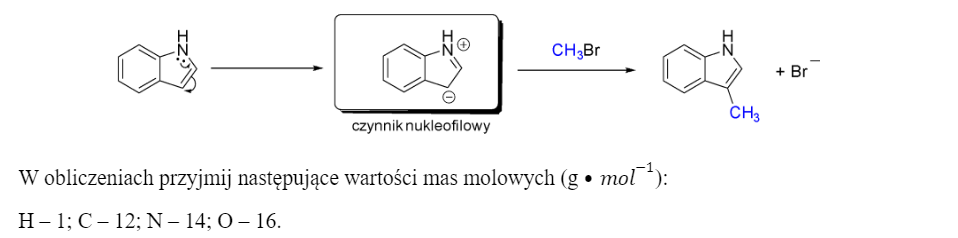
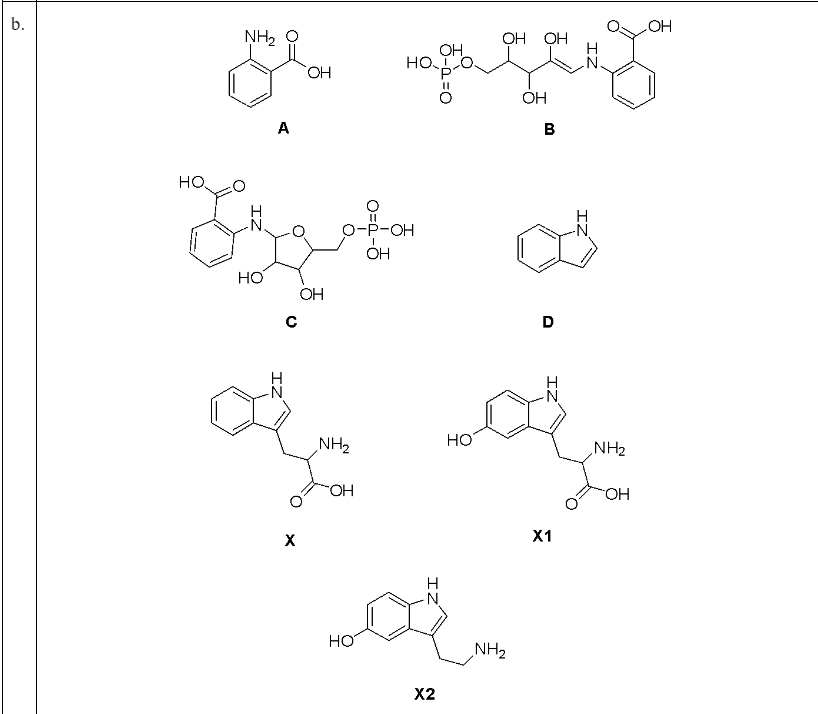
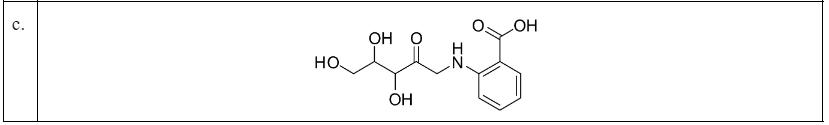
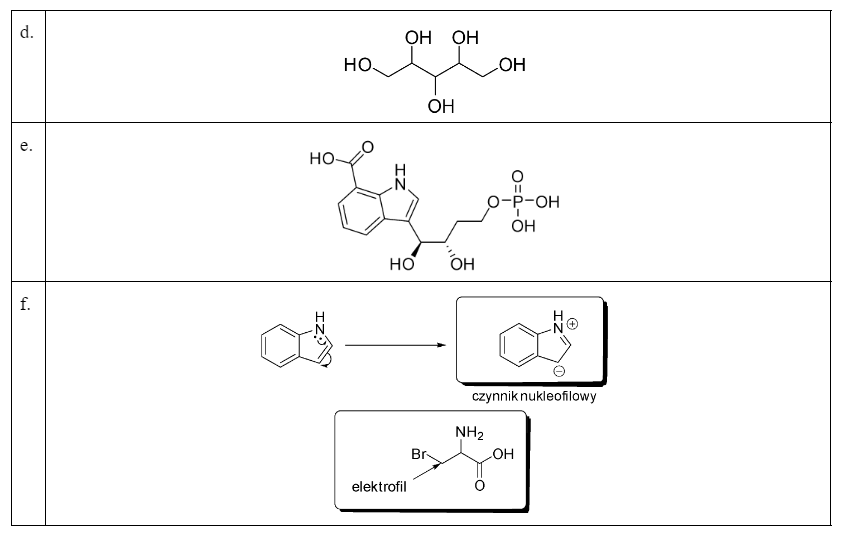
A5 – biochemia (Nienaturalne aminokwasy)
Rok temu w folderze wstępnym (zadanie A6) również pojawiło się zadanie dotyczące nienaturalnych aminokwasów. Zamieszczam zatem zeszłoroczną analizę folderu :
Aminokwasy w stopniu już wystarczającym na I etap Olimpiady są opracowane tutaj :
- najpierw przeczytaj o amidach, w których jest obecne wiązanie amidowe, które również jest obecne w peptydach/białkach, które są połączeniem wielu aminokwasów ze sobą
- przechodzimy dalej do mocznika, którego wzór trzeba znać, ale nie tylko tego możemy się tutaj dowiedzieć
- bolączką każdego Olimpijczyka jest bagatelizowanie maturalnych treści, a jakościowe próby na dane związki/grupy funkcyjne to jedne z najpoważniejszych braków, dlatego teraz zobacz co może nam wykryć wodorotlenek miedzi(II). Dobra wiadomość jest taka, że na Olimpiadzie jest mało (i będzie coraz mniej) takich pytań, ponieważ w nowoczesnej chemii takich prób się nie używa (zostały wyparte przez spektroskopię, której będziemy się uczyć do II etapu)
- dochodzimy wreszcie do aminokwasów. Oto, na co szczególnie musisz zwrócić uwagę :
- właściwości kwasowo-zasadowe, ze szczególnym uwzględnieniem jonu obojnaczego (zwitterionu). Musisz umieć napisać dominującą formę w kwasowym, zasadowym i ,,obojętnym” pH.
- definicja punktu izoelektrycznego
- umiesz rysować aminokwasy D oraz L w projekcji Fischera
- podział aminokwasów na kwasowe, zasadowe i obojętne
- połączenie aminokwasów daje nam peptydy, a gdy zrobimy to wiele razy, to powstają nam białka.
- kiedy już to opracujesz tak naprawdę śmiało można już ruszać na zawody. Ale pójdziemy o krok dalej i opowiemy sobie szybko o reakcjach enzymatycznych
- po przerobieniu prezentacji zrób też zadania z ustalania sekwencji peptydów : 57 edycja, I etap : zadanie 5, 67 edycja, folder wstępny : zadanie 6A